武汉伊莱瑞特生物科技股份有限公司品牌商
12 年
手机商铺
- NaN
- 0.7000000000000002
- 0.7000000000000002
- 2.7
- 2.7
推荐产品
公司新闻/正文
T细胞体外培养策略:阴性分选+精准激活,破解实验难题
556 人阅读发布时间:2026-03-02 15:00
当前,CAR-T细胞疗法在治疗血液系统恶性肿瘤方面已显示出显著疗效,但在实体瘤治疗中仍面临挑战,部分原因在于T细胞在体外的扩增效率、表型稳定性以及体内持久性有待提高。在T细胞体外培养过程中,通过阴性分选和精准激活来优化T细胞的纯度和表型稳定性是细胞治疗领域,尤其是嵌合抗原受体T细胞(CAR-T)疗法成功的关键环节。
T细胞分选与激活作为体外培养的基础步骤,实操中常面临三大痛点:传统阳性分选易导致外源磁珠残留及抗体结合改变受体构象,引发非特异性活化和表型漂移;固定强度的激活方案易造成T细胞过度刺激、细胞提前耗竭及记忆表型丢失;而分选与激活环节衔接不畅,则会因操作耗时导致细胞活性断崖式下降。
针对这些问题,可采用“阴性分选+精准激活”实现可控刺激,从源头把控T细胞质量、优化后续培养效果的关键策略,如下表所示:
表1. 阴性分选+精准激活的组合策略
| 策略类型 | 核心原理 | 核心优势 | 实操关键要点 |
| 阴性分选 (CD3+T细胞或Pan Naive T细胞) |
通过特异性抗体标记样本中非T细胞(B细胞、单核细胞等),结合磁珠去除非靶细胞,间接富集未被标记的靶T细胞,无需标记T细胞表面受体。 | ●无外源标记与磁珠残留,避免T细胞表面受体构象改变; ●靶T细胞未受额外刺激,活细胞率可达95%以上; ●表型接近体内天然状态,适配后续所有实验(激活、转染、长期培养等); ●分离速度高效,全程仅需20min。 |
●选用CD3+T细胞阴性分选试剂盒,适配PBMC、小鼠脾细胞/淋巴结细胞; ●抗体室温孵育5min,磁珠孵育5min,轻混匀; ●磁分离室温静置5min,仅收集上清液(避免触碰磁珠复合物); ●分选后流式检测纯度≥95.98%、活细胞率≥98%。 注意:新鲜样本细胞得率高,请尽可能使用新鲜的样本。 |
| 精准激活 | 建立“抗CD3/CD28 Beads高效刺激链接细胞因子扩增培养”的可控体系,遵循“适度激活启动增殖,精准调控维持表型”原则,避免传统强刺激损伤细胞。 | ●避免过度激活导致的T细胞提前耗竭; ●有效维持记忆表型(TN/TCM),减少耗竭标志物(PD-1、LAG3)表达; ●激活效率稳定,适配后续长期培养与细胞治疗研发需求。 |
●基础刺激:使用CD3/CD28 Beads和CD3+T细胞按合适的比例混合,激活3-5天后采用磁吸法去除CD3/CD28 Beads,可磁吸两次充分去除激活Beads; ●细胞因子扩增培养:初期低剂量IL-2(50 U/mL)培养细胞,24h后添加IL-7、IL-15(各5ng/mL);细胞传代密度调整为5×10^5/mL,每48h换液培养,同时补充细胞因子。 |
注意:两种策略需无缝衔接,尽量选用新鲜样本进行分选,分选后30-60 min内快速加入CD3/CD28 Beads进行激活体系搭建,全程减少细胞室温暴露与过度吹打,守住细胞活性与表型稳定性;此外,过高的IL-2会导致T细胞发生衰竭,前期激活过程可不加IL-2,后续激活后培养IL-2浓度不要超过50 U/mL。
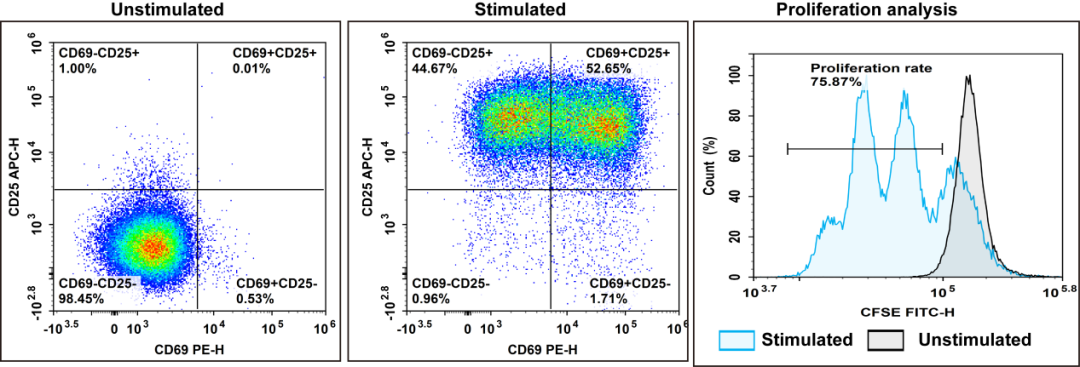
图1. 人CD3+T细胞的阴性分选和快速激活实验结果。人外周血细胞使用Human PBMC Separation Solution(P1.077)(E-CK-A103)分选出PBMC细胞后,使用EasySort™ Human CD3+T Cell Isolation Kit(MIH001N)分选出纯度为98.2%的CD3+T细胞,经CFSE Cell Division Tracker Kit(E-CK-A345)染色后,使用Human CD3/CD28 T Cell Activation Beads(MIH001A)激活培养72 h后检测细胞激活效率。
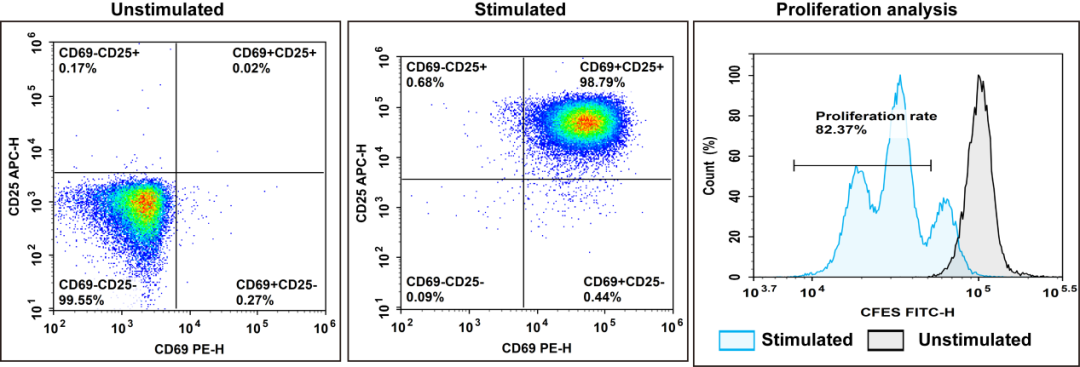
图2. 人Naïve Pan T细胞的阴性分选和快速激活实验结果。人外周血细胞使用Human PBMC Separation Solution(P1.077)(E-CK-A103)分选出PBMC细胞后,使用EasySort™ Human Naïve Pan T Cell Isolation Kit(MIH006N)分选出纯度为98.2%的CD3+T细胞,经CFSE Cell Division Tracker Kit(E-CK-A345)染色后,使用Human CD3/CD28 T Cell Activation Beads(MIH001A)激活培养72 h后检测细胞激活效率。
阴性分选+精准激活的组合策略实验流程复杂,涉及众多细节操作,常见问题和解决方案和避坑指南如下所示:
☑ 常见问题一:阴性分选后CD3+纯度<90%
核心原因
-
死细胞未去除;
-
抗体/磁珠孵育时间不足;
-
磁分离不充分。
针对性解决方案
-
提前用死细胞去除试剂盒处理样本;
-
按照产品说明书反馈合理延长孵育时间(抗体20 min、磁珠10 min);
-
磁力架不配套或磁力不够,适当增加磁分离静置时间,可重复磁分离1次。
☑ 常见问题二:激活后细胞活率<80%
核心原因
-
分选-激活衔接耗时超30 min;
-
培养基/试剂未预温;
-
初始细胞密度不当。
针对性解决方案
-
使用新鲜的样本,严格按照说明书操作,30 min内完成激活,避免过度吹打细胞;
-
所有试剂提前37℃预温;
-
调整密度至5×105/mL,使用超低吸附培养板可以减少细胞在培养过程中的非特异性吸附,24 h后半量补液,48 h全换液体并补加细胞因子,以维持培养基中营养物质和细胞因子的浓度,确保T细胞持续扩增。
☑ 常见问题三:激活后表型漂移,记忆表型比例大幅下降
核心原因
-
CD3/CD28 Beads比例过高或激活时间过久;
-
未加IL-7+IL-15;
-
培养初期IL-2剂量过高。
针对性解决方案
-
适当减少CD3/CD28 Beads比例,降低激活时间到3 h,最长不要超过5天 ;
-
适当添加IL-7+IL-15组合因子;
-
IL-2控制在50 U/mL以内,高剂量会引起细胞衰竭。
☑ 常见问题四:激活后细胞增殖缓慢,无明显聚团
核心原因
-
刺激强度不足或刺激过强;
-
缺共刺激分子;
-
培养条件异常。
针对性解决方案
-
调整合适的CD3/CD28 Beads比例和激活时间,镜下观察可看到清晰的细胞聚团;
-
添加CD27/CD137(4-1BB)共刺激分子和IL-7/IL-15/IL-2细胞因子;
-
检查培养箱,避免培养板密封过严缺氧。
T细胞体外培养的关键在于获得高纯度、表型稳定且活性优异的T细胞。阴性分选结合精准激活的策略,从原理上解决了外源残留、表型不稳定等核心问题。再配合标准化的操作流程、细致的环节控制与系统化的问题排查,实现高质量T细胞的获取。
您在T细胞体外培养中还遇到过哪些实操难题?欢迎在评论区留言交流。后续我们将持续分享T细胞长期培养的关键要点,详细解读如何在21天培养周期中获得更高活力的T细胞,敬请期待!
参考文献:
[1] Deckers, J., Anbergen, T., Hokke, A. M., de Dreu, A., Schrijver, D. P., de Bruin, K., Toner, Y. C., Beldman, T. J., Spangler, J. B., de Greef, T. F. A., Grisoni, F., van der Meel, R., Joosten, L. A. B., Merkx, M., Netea, M. G., & Mulder, W. J. M. (2023). Engineering cytokine therapeutics. Nature Reviews Bioengineering, 1(4), 286–303.
[2] Chan, J. D., Lai, J., Slaney, C. Y., Kallies, A., Beavis, P. A., & Darcy, P. K. (2021). Cellular networks controlling T cell persistence in adoptive cell therapy. Nature Reviews Immunology, 21(12), 769–784.


![FITC Anti-Mouse CD3 Antibody流式抗体[17A2]](https://img1.dxycdn.com/p/s14/2025/0609/471/0481799173518002391.png!wh200)
![FITC 标记抗小鼠/人 CD11b 抗体-流式抗体[M1/70]_货号:E-AB-F1081C](https://img1.dxycdn.com/p/s14/2025/0609/740/6904673901537002391.png!wh200)