武汉伊莱瑞特生物科技股份有限公司品牌商
12 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.7000000000000002
- 0.7000000000000002
- 2.7
- 2.7
Elabscience Aptplex™ 人免疫耐受相关12指标多因子试剂盒:精准解析Th1/Th2/Treg免疫平衡,助力免疫耐受机制研究
¥17430
推荐产品
公司新闻/正文
Elabscience CCK-8实验避坑指南:常见FAQ与异常结果全解析
253 人阅读发布时间:2026-04-20 16:54
做细胞实验的小伙伴,对 CCK-8 实验肯定不陌生。细胞实验中经常通过 CCK-8 实验进行细胞增殖和毒性分析。本期为大家整理了 CCK-8 常见 FAQ 清单,并结合真实案例进行异常结果分析,助力获取满意实验结果。
一、CCK-8 检测原理
粉色的WST-8在电子载体1-Me-PMS的作用下,可被细胞中的脱氢酶还原成为黄色的甲瓒产物,该产物在450 nm波长处有特征吸收峰。吸光度变化速率,即甲瓒生成速率与脱氢酶活性呈正比,间接反应了活细胞数量,可利用这一特性直接进行细胞增殖和毒性分析。
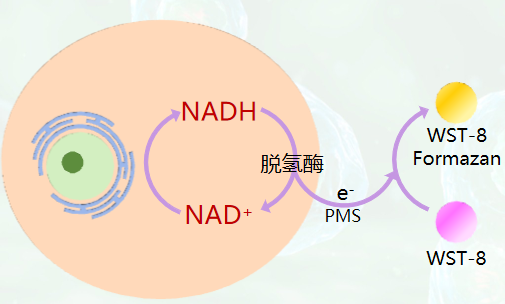
二、不同细胞增殖和毒性分析检测方案对比
表格
| 方法 | MTT | XTT | WST-1 | CCK-8 |
|---|---|---|---|---|
| 甲臜的溶解度 | 不溶 | 水溶 | 水溶 | 水溶 |
| 形式 | 粉末 | 液体 | 液体 | 液体 |
| 使用方法 | 溶解后使用 | 提前准备 | 直接使用 | 直接使用 |
| 灵敏度 | - | ++ | ++ | ++ |
| 检测范围 | 560-600 nm | 420-480 nm | 420-480 nm | 430-490 nm |
| 细胞毒性 | + | - | - | - |
| 稳定性 | - | - | + | ++ |
| 可重复性 | - | - | +++ | - |
| 便捷性 | - | - | - | - |
从对比可知,CCK-8 在水溶性、灵敏度、检测速度和细胞毒性等方面均优于 MTT。
三、CCK-8 检测结果展示
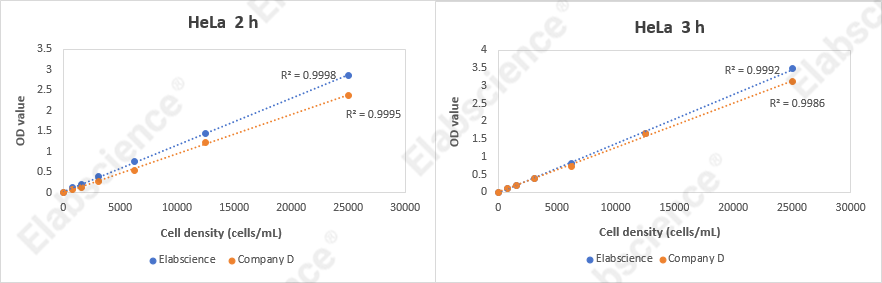
图2. CCK-8检测实验结果图。将不同密度的HeLa细胞(25000、12500、6250、3125、1562、780、390、0个细胞/mL)接种至96孔板中,于37℃培养24小时,随后分别使用增强型细胞活力检测试剂盒(CCK-8)(E-CK-A362)孵育2小时和3小时,并在450 nm波长下测定OD值。
结果分析示例
表格
| 分组 | OD 值 | 平均值 | 减空白 | 存活率 |
|---|---|---|---|---|
| 空白组 | 0.1986、0.2049、0.2052 | 0.2029 | - | - |
| NC 组 | 1.2725、1.2655、1.2058 | 1.2479 | 1.0450 | 100% |
| 处理组 1 | 0.9847、0.9554、1.0351 | 0.9917 | 0.7888 | 75.48% |
| 处理组 2 | 0.9079、0.9543、0.9238 | 0.9287 | 0.7258 | 69.45% |
| 处理组 3 | 0.8154、0.862、0.8398 | 0.8391 | 0.6362 | 60.88% |
| 处理组 4 | 0.6335、0.6345、0.6638 | 0.6439 | 0.4410 | 42.20% |
计算公式
细胞存活率(%)=(ODsample-ODblank)/(ODcontrol -ODblank)× 100%
- ODsample:实验孔 OD 值
- ODcontrol:对照孔 OD 值
- ODblank:空白孔 OD 值
四、实验常见 FAQ
Q1:每孔应该加多少细胞?
需根据细胞大小、增殖速度决定。
- 细胞增殖实验:100 μL 约含2000 个细胞
- 细胞毒性实验:100 μL 约含5000 个细胞
Q2:CCK-8 加入后,孵育时间如何确定?
- 每孔加 10 μL CCK-8 溶液,继续孵育1-4 h(与细胞培养条件相同)。
- 判断标准:每隔半小时观察,对照组孔变为橙黄色即可终止;时间过短信号弱,过长易 OD 值饱和。
Q3:CCK-8 试剂如何保存?反复冻融有影响吗?
- 保存:避光 - 20℃或 4℃;长期 - 20℃,短期 4℃分装保存(1-2 周用完)
- 反复冻融会降低灵敏度,建议单次用量分装
Q4:96 孔板边缘孔结果总是不正常?
- 存在边缘效应:外圈孔蒸发快,培养基浓缩、细胞状态差异大。
- 解决:外圈只加无菌 PBS 或纯培养基,不铺细胞。
Q5:OD 值理想范围是多少?
- 一般:0.2-1.5
- 对照组最佳:0.8-1.2
- OD>2.0:细胞过密或显色时间过长;OD<0.2:细胞太少或药物毒性强
Q6:药物本身有颜色 / 易氧化,会影响结果吗?
会。需设置无细胞 + 药物 + CCK-8背景对照孔,计算时扣除对应背景 OD 值。
Q7:CCK-8 可以回收再利用吗?
不建议。回收易导致误差、增加污染风险。
Q8:如何做空白对照?
- 常规:培养基 + CCK-8,不加细胞
- 药物干扰:培养基 + 药物 + CCK-8,不加细胞
Q9:空白孔数值上升?
- 液体挥发导致浓度升高。
- 解决:外圈加培养基 / PBS 保湿;培养箱靠近水盘放置。
Q10:一般多久测一次值?
预实验:0.5、1、2、4 小时分别检测,选取适宜时间点。
Q11:加入 CCK-8 后暂时不测,如何保存?
每孔加 10 μL 0.1M HCl 或 1% SDS 溶液,室温避光,24 小时内吸光度稳定。
Q12:培养基颜色 /pH 变化,需要更换吗?
培养时间较长时,建议更换新鲜培养基再加入 CCK-8。
Q13:CCK-8 适用什么细胞?
- 适用于真核、有线粒体的细胞(动物细胞、单细胞);
- 不推荐:植物、酵母等有细胞壁的细胞(底物进入效率低)。
Q14:可替代 BrdU/EdU 检测增殖吗?
可以。CCK-8 检测脱氢酶反映活性,BrdU/EdU 检测 DNA 合成,二者相关,且 CCK-8 更便捷。
Q15:混合培养细胞,只测一种可行吗?
- 贴壁细胞:移除悬浮细胞后常规检测
- 不可移除:总活性为两者之和;T 细胞量少 / 稳定时,可通过对照扣除影响
五、CCK-8 实验异常结果分析
情况 1:加药后细胞状态差,但 OD 值高于对照组
- 可能原因:药物具有氧化还原性
- 解决方案:设置无细胞 + 药物 + CCK-8背景对照孔
情况 2:镜下细胞基本死亡,OD 值仍偏高
- 可能原因:孔板污染、细胞接种数过高、CCK-8 孵育时间过长
- 解决方案:检查污染、降低接种数、缩短孵育时间
情况 3:所有孔 OD 值约 0.3,不显色
表格
| 情况类型 | 可能原因 | 解决方案 |
|---|---|---|
| 对照组状态好,细胞密度稀 | 接种密度低,未达检测灵敏度 | 增大接种密度 |
| 对照组状态好,培养基有干扰 | 培养基具氧化还原性 | 更换培养基 |
| 对照组状态差,大量死亡 | 接种密度过高,接触抑制 | 降低接种数 |
| 所有组细胞状态均差 | 接种前细胞状态差 | 调整细胞状态 |
以上就是 CCK-8 实验的常见问题解答和异常结果分析,希望能帮大家避开实验坑,轻松做出理想结果!后续还会持续分享更多实操干货,关注Elabscience® ,解锁更多实验小技巧~


![FITC Anti-Mouse CD3 Antibody流式抗体[17A2]](https://img1.dxycdn.com/p/s14/2025/0609/471/0481799173518002391.png!wh200)
![FITC 标记抗小鼠/人 CD11b 抗体-流式抗体[M1/70]_货号:E-AB-F1081C](https://img1.dxycdn.com/p/s14/2025/0609/740/6904673901537002391.png!wh200)